L’Alzheimer è la malattia neurodegenerativa più comune, che colpisce circa 24 milioni di persone nel mondo. Ad oggi è una malattia per la quale non esistono cure efficaci.
Le elevate percentuali di fallimento nei trial clinici per le malattie neurodegenerative come l’Alzheimer sono legate alla scarsa capacità predittiva dei modelli di malattia attualmente basati sugli animali. Questo ha generato una crescente richiesta di modelli alternativi basati sull’uomo, in grado di mimare adeguatamente specifiche caratteristiche della malattia in vitro.
Per affrontare questo problema, la Food and Drug Administration (FDA) ha recentemente approvato l’uso di saggi basati su cellule e modelli informatici nei trial preclinici, attraverso il passaggio del FDA Modernization Act 2.0. A tal fine, negli ultimi anni si è concentrata l’attenzione sullo sviluppo di modelli in vitro basati su cellule umane. I recenti progressi nella bioingegneria e nella tecnologia organ-on-a-chip hanno permesso la creazione di modelli di co-coltura complessi che meglio mimano i processi fisio-patologici in vitro. Ad esempio, è stato recentemente dimostrato che le neurosfere derivate da cellule staminali neurali specifiche dell’Alzheimer portatrici di mutazioni genetiche familiari associate alla malattia, replicano caratteristiche specifiche della malattia in vitro. Allo stesso tempo vi è stato un rapido avanzamento nei modelli che imitano la barriera vascolare del cervello (barriera emato-encefalica).
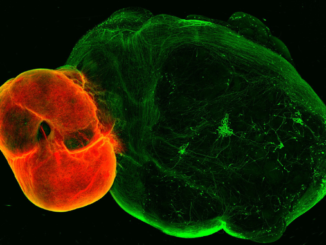
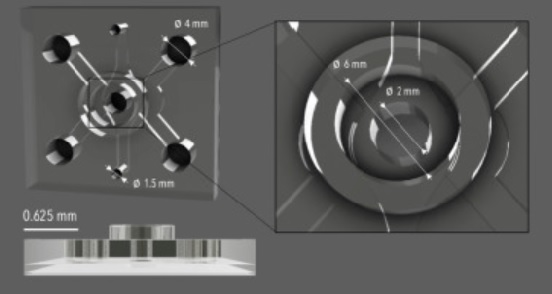
Eunkyung Ko, ricercatore al Massachusetts Institute of Technology di Cambridge (US), e i suoi colleghi hanno sviluppato un modello tridimensionale della malattia di Alzheimer utilizzando un dispositivo microfluidico compartimentato che combina una rete di vasi sanguigni della barriera emato-encefalica umana con “neurosfere” derivate da cellule progenitrici neurali umane, specifiche per l’Alzheimer.
Oltre ai principali segni neuropatologici dell’Alzheimer, come accumuli di proteine chiamate placche di amiloide, grovigli neurofibrillari, perdita neuronale, ecc., in oltre 20 studi post-mortem indipendenti su umani1 si è osservata un’ alterazione della barriera emato-encefalica e della regolazione vascolare. La barriera emato-encefalica è una barriera altamente selettiva formata da cellule endoteliali che rivestono i piccoli vasi sanguigni del cervello, e altre cellule di supporto che regolano il passaggio di molecole tra il flusso sanguigno e il tessuto cerebrale. Un’alterata regolazione di tale barriera può avere effetti dannosi sul tessuto cerebrale, influenzando l’insorgenza e la progressione della malattia, rendendo la BBB un elemento chiave nell’Alzheimer.
Per ridurre i tempi di co-coltura microfluidica, i ricercatori hanno pre-differenziato le neurosfere per 21 giorni per far loro esprimere caratteristiche patologiche specifiche dell’Alzheimer, prima di essere introdotte nel dispositivo microfluidico.
Come confermato dagli studi post-mortem sull’Alzheimer, dopo 7 giorni di co-coltura con neurosfere specifiche pre-differenziate per l’Alzheimer, la rete tridimensionale della barriera emato-encefalica ha mostrato significativi cambiamenti nella permeabilità e nella morfologia. Inoltre, le reti vascolari in co-coltura con piccoli pezzi di tessuto specifici dell’Alzheimer hanno mostrato depositi localizzati di beta-amiloide.
Il modello presentato, affermano gli autori, ha un enorme potenziale per replicare le principali caratteristiche delle malattie neurodegenerative a livello vascolare e neurale.
Gli autori hanno dimostrato con successo un metodo per generare un modello in vitro cmplesso di Alzheimer che riproduce gli aspetti critici della patologia umana. Questo sistema, concludono i ricercatori, offre tempi di co-coltura ridotti, consentendo comunque l’osservazione dei cambiamenti patologici. L’approccio presentato ha un grande potenziale per studiare il ruolo della barriera emato-encefalica nell’insorgenza e nella progressione di varie malattie neurodegenerative (ad esempio, Alzheimer, Parkinson o corea di Huntington) e per studi di screening dei farmaci.
Note:
- Fonte: https://www.mdpi.com/1422-0067/24/22/16288
Per approfondimenti:
Ko, E. C., Spitz, S., Pramotton, F. M., Barr, O. M., Xu, C., Pavlou, G., Zhang, S., Tsai, A., Maaser-Hecker, A., Jorfi, M., Choi, S. H., Tanzi, R. E., & Kamm, R. D. (2023). Accelerating the in vitro emulation of Alzheimer’s disease-associated phenotypes using a novel 3D blood-brain barrier neurosphere co-culture model. Frontiers in bioengineering and biotechnology, 11, 1251195.