Nel 1012 il medico persiano Ibn Sina, disquisendo in merito all’utilizzo di animali per lo sviluppo di medicamenti ad uso umano, aveva lanciato questo monito: “gli esperimenti devono essere eseguiti sul corpo umano. Se sono eseguiti sugli animali il rischio di fallire è duplice: una medicina potrebbe essere calda in riferimento al corpo umano e fredda rispetto a quello di leone o di un cavallo…..la seconda ragione sta nel fatto che la qualità della medicina potrebbe avere sul corpo umano effetti differenti da quelli visti negli animali”.
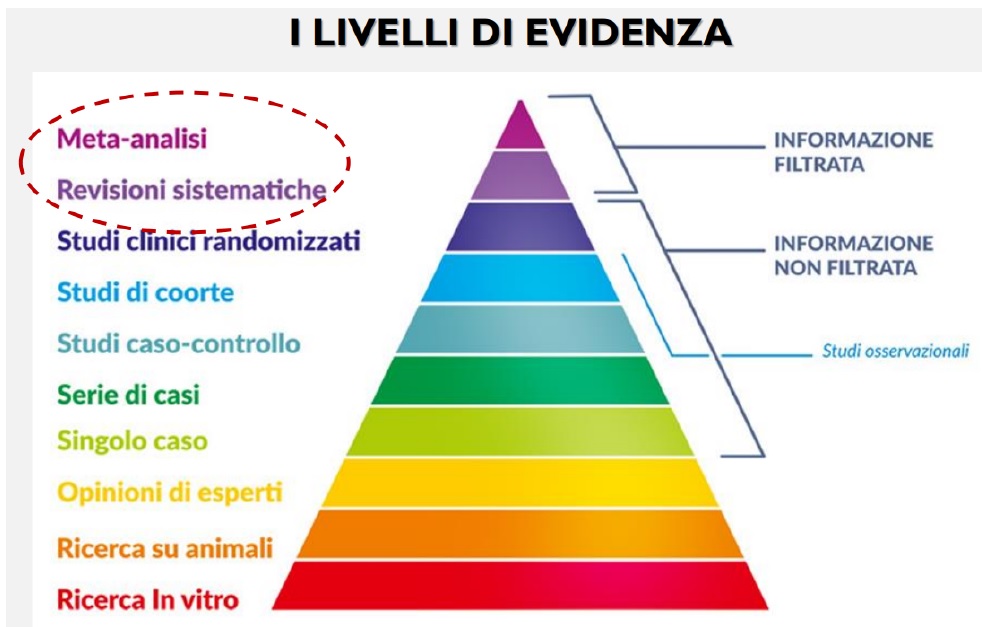
L’attualità di queste parole si è potuta meglio apprendere un millennio dopo, quando soprattutto a partire dal 1989 ma maggiormente dal 2000 in poi, si è fatta largo l’idea della revisione sistematica dei materiali di ricerca. Lo scopo è quello di riesaminare anche alla luce dei risultati clinici, la validità delle ricerche e poter così valutare prospetticamente e sinteticamente (valutazione di tutto il materiale riferito a quel dato argomento) tutto quanto è stato prodotto in un’ottica critica e pragmatica. Nel 2004 Pound et al. pubblicano un articolo intitolato “Dove sono le evidenze che la ricerca sugli animali ha effetti benefici per l’uomo?”. Gli autori sostengono che ci sono pochi dati a sostegno dell’uso degli animali nella ricerca e che mediante la revisione sistematica degli studi su animali si possa rispondere efficacemente alla domanda iniziale da cui sono partiti. Sebbene inizialmente la reazione più comune da parte della stessa comunità scientifica sia stata di forte critica e di prosecuzione dell’asserzione più spesso immotivata delle ragioni pro utilizzo degli animali nella ricerca, il documento ha consentito l’avvio di una serie di revisione sistematiche di studi preclinici condotti su animali. Non solo, sempre nel 2004, all’Università di Edimburgo sotto la guida del neurologo Macleod nacque il CAMARADES (Collaborative Approach to Meta-Analysis and Review of Animal Data from Experimental Studies). Il progetto nacque con lo scopo di revisionare i materiali di ricerche che prevedevano l’utilizzo in ambito preclinico degli animali e ben presto si trovò a sostenere a sua volta altri progetti che si muovevano in tal senso. Si prese le mosse dagli studi preclinici sui farmaci post ischemici, ma si estese ben presto lo studio anche ad altre patologie. Attualmente il progetto, con cinque centri di coordinamento nazionali e partecipanti da tutto il mondo, continua la sua attività di revisione e meta analisi delle ricerche su animali. Nel 2007 sono stati pubblicati i risultati della revisione e del confronto tra studi condotti su animali in fase preclinica e studi clinici sull’uomo. Sono state prese a riferimento 6 diverse aree di patologia, i cui effetti sull’uomo erano ben conosciuti sulla base delle revisioni operate: corticosteroidi per danno cerebrale, corticosteroidi prenatali per distress respiratorio neonatale, bifosfonati per l’osteoporosi, antifibrinolitici per le emorragie, trombolitici e agenti neuroprotettivi (tirilazad) per gli ictus. A questo punto sono stati raccolti ed esaminati tutti gli studi condotti su animali per i medesimi argomenti (pubblicati e non) e sono stati sottoposti a revisione. I risultati sono stati i seguenti:
-i bifosfonati per l’osteoporosi e i trombolitici per l’ictus davano effetti concordi negli studi sugli animali e in quelli clinici sull’uomo;
-i corticosteroidi prenatali usati contro il distress nel parto prematuro, si sono tradotti in risultati solo parzialmente concordanti negli studi;
-mentre i corticosteroidi per il danno cerebrale, gli antifibrinolitici per le emorragie e il Tirilazad come neuroprotettivo in corso di ictus, hanno mostrato sugli animali effetti totalmente discordi da quelli conosciuti nell’uomo.
Nel 2006 la veterinaria Merel Ritskes-Hoitinga fonda il centro 3R (Replacement, Reduction, Refinement) che però a suo avviso non sarà in grado di dare le risposte sperate e dunque insieme ad altre eminenti figure nel 2012 fonda all’università di Radboud in Olanda, il SYRCLE ovvero il centro di revisione sistematica per la sperimentazione sugli animali da laboratorio. Dall’introduzione del metodo di revisione sistematica si è calcolato che gli animali utilizzati nel laboratorio dell’Università siano diminuiti del 35%, mentre nell’intero paese del 15%.
Gli studi di revisione sistematica operati da varie figure tra cui Hoitinga, hanno portato negli anni ad evidenziare quanto segue:
-le ricerche condotte in fase preclinica sugli animali sono spesso di scarsa qualità e tendono ad omettere tutta una serie di dati che potrebbero mostrare le reali differenze in essere con l’uomo;
-la teorizzazione della ricerca è scadente e l’impianto scientifico seguito spesso poco rigoroso, con risultati poco affidabili e dunque con una clinica poco rilevante;
-vengono evidenziati solo i risultati e gli outfit positivi, che ricevono così eccessivo peso e significato nel computo globale (questo sia nei report, che nelle presentazioni rivolte ad enti di valutazione);
-i report sono incompleti con dati mancanti come ad esempio il numero di animali utilizzati, il numero di quelli deceduti o degli esclusi;
-si utilizzano più spesso piccoli animali, con risultati finali scarsamente traslabili al genere umano;
-la numerosità del campione in uso è inappropriata;
-si assiste ad una crisi della riproducibilità, gli esperimenti infatti non sono ripetibili;
-la traslabilità animale-uomo varia da 0 a 100 in modo casuale, senza fattori che ne possono aumentare la predittività;
Dalla collaborazione di Pound e Hoitinga ne è derivata nel 2018 una chiara affermazione che ribadiva come quand’anche tutti i problemi di validità interna (metodologie di ricerca, progetto, report etc) inerenti alla ricerca sugli animali venissero risolti, le differenze di specie sarebbero tali da non consentire ugualmente la loro applicazione sull’uomo.
Sappiamo oggi che la ricerca preclinica sugli animali manca non solo di validità interna ma altresì esterna, ovvero in ragione delle differenze di specie e dell’impossibilità di riprodurre la complessità delle patologie umane. Ma se l’evidenza sulle nuove metodologie human based dovrebbe aver già da tempo per lo meno indotto riflessioni sui modelli in uso, pare che i ricercatori siano in proposito piuttosto riluttanti ad abbandonare i vecchi modelli. Ottanta ricercatori che si occupano comunemente della ricerca sugli ictus, sono stati intervistati sulle problematiche esistenti nella ricerca preclinica in ragione delle differenze di specie, di tutti loro uno soltanto uno ha detto di aver spostato il suo focus d’attenzione su metodologie incentrate sull’uomo. Ma le cose stanno cambiando, assistiamo alla chiusura dei laboratori di sperimentazione animale di alto profilo nel Regno Unito, all’Olanda che è in primo piano nella corsa alla transizione verso una ricerca human based, all’impegno degli Stati Uniti nel porre fino all’impiego degli animali nei test di tossicità e ancora al voto in Europa lo scorso settembre 2021 per sviluppare un piano coordinato, volto a rimpiazzare gli esperimenti su animali con metodologie innovative che prescindano dal loro impiego. Gli autori si chiedono se tutto ciò non sia il preludio di una rivoluzione scientifica in arrivo.
Fonti:
Ritskes-Hoitinga M, Pound P (2022). The role of systematic reviews in identifying the limitations of preclinical animal research, 2000 – 2022. JLL Bulletin: Commentaries on the history of treatment evaluation (https://www.jameslindlibrary.org/articles/the-role-of-systematic-reviews-in-identifyingthe-limitations-of-preclinical-animal-research-2000-2022/)
Pound P, Ritskes-Hoitinga M. Is it possible to overcome issues of external validity in preclinical animal research? Why most animal models are bound to fail. J Transl Med. 2018;16(1):304. Published 2018 Nov 7. doi:10.1186/s12967-018-1678-1



