Nel percorso verso l’implementazione di terapie promettenti contro il cancro, dal banco del laboratorio al paziente, un momento cruciale consiste nell’analizzare la sicurezza di tali composti nell’uomo. Tradizionalmente, questa valutazione inizia con studi di tossicità preclinici in modelli animali come topi, ratti, cani e scimmie. Tuttavia, uno studio recente mette in luce una discrepanza preoccupante tra le tossicità osservate in questi studi sugli animali e quelle riscontrate nei trial clinici di fase precoce che coinvolgono pazienti affetti da cancro.
Lo studio, condotto da ricercatori di due importanti centri di trial clinici di fase precoce, ha analizzato i dati relativi a 108 farmaci testati nei trial clinici oncologici di fase 1. Questi farmaci comprendevano una varietà di composti, incluse piccole molecole, farmaci biologici e coniugati. I ricercatori hanno confrontato le tossicità precliniche documentate nei fogli informativi delle sperimentazioni con le tossicità cliniche riportate nei trial clinici di fase 1 pubblicati.
I risultati hanno rivelato una mancanza di correlazione tra la tossicità osservata nei modelli animali e quella sperimentata dai partecipanti umani. Le analisi statistiche, inclusi i valori predittivi positivi (PPV) e i valori predittivi negativi (NPV), hanno indicato che la capacità dei test preclinici su animali di predire la tossicità umana era scarsa. Il PPV mediano era dello 0,65, suggerendo che circa due terzi delle tossicità osservate negli animali erano state osservate anche negli esseri umani. Tuttavia, il NPV dello 0,50 indicava che la metà delle tossicità assenti nei modelli animali si manifestavano comunque nei trial umani.
Questi risultati sono preoccupanti, poiché mettono in discussione l’affidabilità dei paradigmi attuali di test di tossicità preclinica nel predire le risposte umane alle terapie sperimentali contro il cancro. Nonostante decenni di affidamento sui modelli animali per i test di tossicità, i risultati osservati in questo studio mettono in luce i limiti di questi approcci.
Inoltre, l’assenza di correlazione persisteva tra vari tipi di composti e differenti livelli di gravità della tossicità, come valutato attraverso i sistemi di classificazione clinica. Questo suggerisce che la discrepanza non è limitata a specifiche categorie di farmaci o a particolari livelli di tossicità, ma rappresenta piuttosto una sfida generale nel processo di traslazione dalla ricerca preclinica all’applicazione clinica.
Le implicazioni di questa discordanza sono di ampia portata. Non solo solleva preoccupazioni etiche riguardanti l’uso degli animali nella ricerca se il loro valore predittivo è limitato, ma ha anche implicazioni pratiche per lo sviluppo di farmaci. L’incapacità di predire accuratamente la tossicità umana può comportare effetti avversi inaspettati nei trial clinici, portando a ritardi, costi maggiori e, soprattutto, potenziali danni ai pazienti.
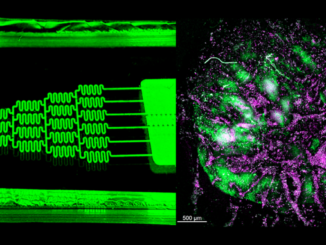
Alla luce di questi risultati, c’è un urgente bisogno di rivalutare gli approcci attuali ai test di tossicità preclinica. I ricercatori e gli sviluppatori di farmaci devono esplorare metodologie innovative che offrano una migliore capacità predittiva per l’indagine umana. Ciò dovrebbe comportare l’adozione di modelli in vitro avanzati, come gli organoidi o i sistemi microfisiologici, che mimano meglio la fisiologia umana e consentono una valutazione più precisa della tossicità.
Inoltre, lo sviluppo di modelli computazionali e algoritmi di apprendimento automatico offre la promessa di migliorare le capacità predittive dei test preclinici. Sfruttando grandi set di dati provenienti sia da studi preclinici che clinici, questi strumenti possono identificare pattern e relazioni che potrebbero non essere evidenti attraverso metodi tradizionali.
In definitiva, affrontare la discrepanza tra tossicità animale e umana richiederà uno sforzo concertato da parte degli attori della comunità scientifica. Iniziative collaborative volte a perfezionare i protocolli di test preclinici e ad adottare tecnologie innovative sono passi essenziali verso la garanzia la sicurezza e l’efficacia delle terapie contro il cancro per i pazienti.
In conclusione, mentre gli studi di tossicità preclinica rimangono un fondamento dello sviluppo dei farmaci, i loro limiti nel predire le risposte umane sottolineano la necessità di innovazione ed evoluzione in questo campo. Abbracciando nuovi approcci e tecnologie, possiamo migliorare la rilevanza traslazionale della ricerca preclinica e aumentare il tasso di successo dei trial clinici oncologici, portando benefici ai pazienti.
Bibliografia
Atkins JT, George GC, Hess K, Marcelo-Lewis KL, Yuan Y, Borthakur G, Khozin S, LoRusso P, Hong DS. Pre-clinical animal models are poor predictors of human toxicities in phase 1 oncology clinical trials. Br J Cancer. 2020 Nov;123(10):1496-1501.
Hockney, S., Parker, J., Turner, J. E., Todd, X., Todryk, S., Gieling, R. G., Hilgen, G., Simoes, D. C. M., & Pal, D. (2023). Next generation organoid engineering to replace animals in cancer drug testing. Biochemical pharmacology, 213, 115586.
https://www.re-place.be/news/non-animal-models-immuno-oncology
Pistollato, F., Bernasconi, C., McCarthy, J., Campia, I., Desaintes, C., Wittwehr, C., Deceuninck, P., & Whelan, M. (2020). Alzheimer’s Disease, and Breast and Prostate Cancer Research: Translational Failures and the Importance to Monitor Outputs and Impact of Funded Research. Animals : an open access journal from MDPI, 10(7), 1194.